Cílovým objemem je primární tumor (lůžko tumoru) a postižené uzliny (svodná lymfatická oblast u pooperační radioterapie), některými autory je doporučováno i „preventivní“ ozáření rizikových lymfatických uzlin i přes absenci známek jejich postižení nádorovým onemocněním.
Režimy vhodné pro protonovou terapii, zejména u lokálně pokročilých NSCLC, umožňují zvýšení jednotlivých dávek na frakci a zkrácení celkové ozařovací doby (stejná nebo vyšší biologicky ekvivalentní dávka). U časných karcinomů lze vzhledem k dozimetrickým výhodám volit stejný frakcionační režim pro centrální i periferní tumory.
Pro protonovou radioterapii je zajištění reprodukovatelnosti stejné polohy a tím i cílového objemu, který se bude ozařovat zcela zásadní. Aby se zabránilo nechtěným pohybům v souvislosti s dýcháním, využíváme v PTC techniku tzv. řízeného dýchání, tj. zadržování dechu v hlubokém nádechu (Deep Inspiration Breath Hold, DIBH). Dýchací pohyby jsou sledovány pomocí přístroje Dyn´R, který měří množství nadechovaného a vydechovaného vzduchu. Systém se skládá ze spirometru, náustku, nosní svorky (k zabránění unikání vzduchu mimo spirometru) a speciálních brýlí.
Tento způsob umožňuje minimalizovat dechové pohyby, a tím ozářit nádor vysokou dávkou s maximální přesností a zároveň s minimálním ozářením zdravé části plíce, druhé plíce, srdce, srdečních cév a orgánů v mediastinu. Protonová léčba tak výrazně zvyšuje poměr mezi šancí na kontrolu nádoru, tedy zvýšení efektu léčby a redukcí možných závažných nežádoucích účinků.
Protonová radioterapie zajistí výbornou dávkovou distribuci u pacientů s časným stadiem NSCLC, při vysoké lokální kontrole a přežití. Pacienti s časnými stadii onemocnění, centrálně uloženými tumory nebo v blízkosti plexus brachialis mají největší benefit z protonové RT.
Tabulka č. 1: Srovnání frakcionačních režimů v léčbě NSCLS lokalizovaného/pokročilého karcinomu
| Režim | Dávka (Gy) | Počet frakcí/Počet frakcí/dávka na frakci (Gy) | Celková doba (týdny |
| Fotony | 74.0 | 37 x 2.0 Gy | 7,4 |
| Protony (lokálně pokročilé onemocnění) | 67.5
54.0 |
25 x 2,7 Gy
18 x 3 Gy |
5
3,5 |
| Protony (lokalizované nádory) | 60.0
70.0 |
10 x 6 Gy
10 x 7 Gy |
2
2 |
U časného karcinomu léčeného SBRT nabízí protonová terapie možnost ozářit cílový objem konformně za použití méně polí (ve srovnání s fotonovou IMRT) a tím snížit integrální dávku. Snížení integrální dávky provází menší riziko stochastických účinků, tzn. menší riziko rozvoje radiační pneumonitidy, ezofagitidy a druhotných tumorů. Dále se snižuje dávka na kritické orgány, zejména plicní tkáň.
U lokálně pokročilého karcinomu plic je protonová terapie lepší než fotonová a nabízí možnost akcelerace (zkrácení celkové doby ozařování), použití menšího počtu léčebných frakcí (hypofrakcionace), zvýšení celkové dávky za současné stejné nebo nižší toxicity (menší zatížení kritických orgánů při stejné dávce ve srovnání s fotonovou radioterapií) a tím zvýšení kvality života pacientů. Stejně jako u časného karcinomu je další výhodou nižší integrální dávka ve srovnání s fotonovým zářením.
U pacientů s nemalobuněčným karcinomem plic při eskalaci dávky bylo prokázáno zlepšení lokální kontroly a přežití. V důsledku fyzikálních vlastností (Braggův peak) dochází k minimalizaci výstupní dávky, což vede k šetření kritických tkání jako jsou srdce, jícen, hlavní dýchací cesty, velké cévy a mícha, ve srovnání s fotonovou RT. Snížení toxicity u protonové radioterapie (PRT) vede ke snížení nákladů na léčbu vedlejších účinků a tím se snižují náklady na hospitalizaci pacienta. Optimalizace dávek vede k šetření zdravých tkání i u pacientů se složitými anatomickými poměry.
Z recentních prací je zřejmé, že protonová radioterapie je efektivní a bezpečná u pacientů s centrálně uloženým NSCLC I stadia. Dále, tumory lokalizované v apexu plic, v blízkosti plexus brachialis lze lépe ozářit PRT při šetření okolních zdravých tkání. U pacientů s bilaterálním časným stadiem NSCLC je zajištěna lepší dávková distribuce při PRT v porovnání s jinými terapeutickými modality. Několik klinických studií potvrzuje, že PRT zajistí dodání adekvátní dávky i u lokálně pokročilých onemocnění. Prospektivní randomizované studie ukazují, že zlepšení lokální kontroly při konkomitantní chemoradioterapii zvyšuje celkové přežití .
Následující obrázek č. 1 a tabulka č. 2 jsou příkladem ozařovacího plánu a dávkové distribuce na jednotlivé orgány. Řezy na plánovacím CT ukazují rozložení dávky v normální a nádorové tkáni. Pro protony je pouze 1/6 dávky v nádoru aplikována do pravé plíce a levá plíce je zcela chráněna před nežádoucím ozářením.
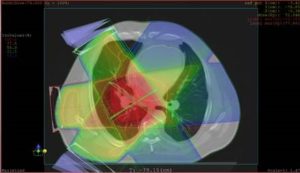
fotonová IMRT radioterapie
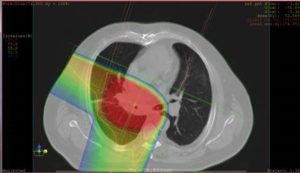
protonová IMPT radioterapie
Tabulka č. 2: Dávka na plíce a míchu ve srovnání s dávkou do nádoru
| 3-D RT (fotony) | IMPT (protony) | |
| Cílový objem (plicní nádor) | 74 Gy (100%) | 74 Gy (100%) |
| Plíce (Dmean) | 19,7 Gy (26%) | 8,8 Gy (11,8%) |
| Mícha (Dmax) | 53 Gy (71%) | 8,1 Gy (10,9%) |
Kniha k zakoupení prostřednictvím odkazu níže.